|
生体から取り出した細胞を培養するとき、培養器に接着できない細胞は増殖できず、速やかに細胞死のプログラムを作動させて死滅する。この「細胞増殖の足場依存性」はすべての動物細胞が持つ進化的に保存された属性である。生体内では、細胞は細胞外マトリックス(extracellular matrix:ECM)とよばれる構造物を足場としている。ECMには様々な接着分子が含まれており、細胞ごとに足場とする接着分子は異なっている。幹細胞のような培養が難しい細胞では、足場の選択が培養の成否を決めると言っても過言ではない。
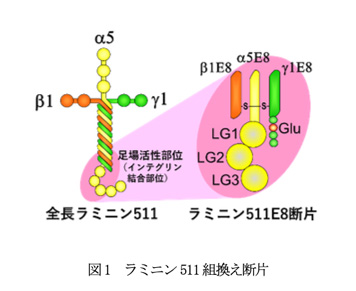
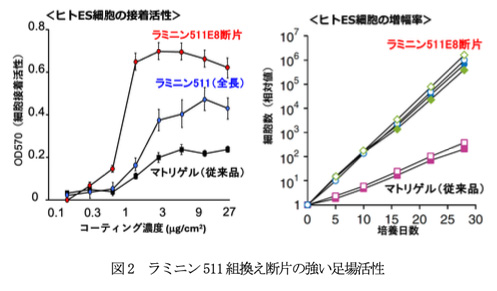
医療応用が期待されているiPS細胞等のヒト多能性幹細胞は足場依存性が特に強く、従来マウス由来哺育細胞を足場として培養されてきた。しかし、この方法では動物由来成分の混入が避けられず、加えて多能性を維持したまま安定的に培養するには操作に熟練する必要があった。受賞者は、マウス初期胚の多能性幹細胞の足場となっているECMの組成を網羅的に解析し、ラミニン511と呼ばれるタンパク質が足場として使われていることを見いだした。さらに、その足場活性を保持した組換え断片の開発に成功し、これを培養基材として使うことで、ヒト多能性幹細胞を安定的かつ効率的に増幅する培養技術を確立した。このラミニン511組換え断片はこれまで報告されたどの培養基材よりもヒト多能性幹細胞に対する足場活性が強く、従来禁忌とされてきた単一細胞分散での継代が可能であり、非熟練者でも安定的にヒト多能性幹細胞を培養・増幅することが容易である。
本技術は京都大学における臨床用iPS細胞およびES細胞の樹立・維持に採用されており、これらの細胞を使った様々な再生医療研究において細胞培養・細胞加工の基盤技術として広く利用されている。わが国で先行しているパーキンソン病、加齢黄斑変性、角膜疾患の臨床研究では、iPS細胞の培養、増幅、分化誘導の全工程においてラミニン511組換え断片が培養基材として使われている。本技術は海外でも着実に普及しつつあり、将来的に多能性幹細胞用培養基材の世界標準となることが期待される。
|


















